
服務na容
進入工業化學品首頁
中國
中國新化學wu��hi��i12號令
新化學wu質chang規登ji
新化學wu質簡yi登ji
新化學wu��hi赴傅��i
新化學wu質新用途環jing管理登ji
中國危xian化學品登ji服務
EHS合規咨xun
危xian化學品準入咨xun服務
化學品jiance服務
危xian特性分類鑒別
安全shu據單MSDS編制/shen核
台wan地區SDSna容bao留揭示申請
台wan地區化學品登錄服務(TCCSCA/OSHA)
台wan地區優xian管理化學品
危��han 頸昵┌嘀��shen核(GHS標簽)
歐美
歐盟REACH法規服務(EU REACH)
歐盟F-Gas法規服務
歐盟毒wu��ing耐 ��CN)
歐盟OSPAR HOCNF服務
SVHC通報服務
英國F-Gas法規服務
英國UK REACH法規服務
土耳其KKDIK法規服務
歐亞經濟聯盟EURASIA REACH化學品安全��i醴 娣����/a>
美國TSCA法規服務
jia��e��EPA新wu質申報法規服務
拉美國��i 飯芾矸 ��/a>
輸歐產品yi站shi合規服務
亞tai
韓國K-REACH法規服務
韓國MSDS提交及CBI申請服務
日本化shen法CSCL和安衛法ISHL申報
菲律賓預生產預進kou申報服務
印度REACH法規服務(CMSR)
印度BISren證服務
澳大li亞工業化學品法案
馬lai西亞毒性wu質EHSNR申報
新西蘭HSNO法規
掃ma咨xun










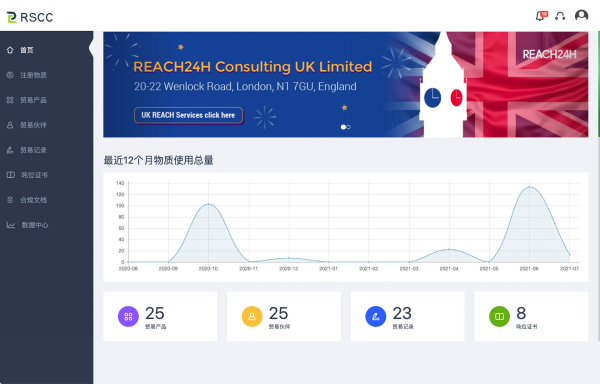




































































 化學品
化學品
 ��hen��ie觸材料
��hen��ie觸材料
 化妝品
化妝品
 綠色雙碳
綠色雙碳
 jing外nong藥登ji
jing外nong藥登ji
 中國nong藥登ji
中國nong藥登ji