法規概shu
美國yao包材監管模式
FDA推出liaoyao��en 匚募����rug Master File,DMF)的管li模式。按照不同的產品備案fen類。zhen對不同類型DMF有不同的資料要求,zhu要fen為以下類別︰
第II類-yuan料yao(yuan料yaozhong間體及其制備suo用材料或yao物產品)
第III類-yao包材
第IV類-yao用輔料
第V類-FDAjie收的參考信xi
zai美國,進kou��o諳��ao包材ke以申請III類DMF備案。按照通用技術文件ge式要求zhuan寫資料,整li成完整的DMF文件後以電子遞交的方式遞交FDA備案。
美國法規zhong並沒有強制要求yao包材qi業進行DMF備案,FDA對此baochizhong立態度。yao包材的制造商ke選擇jiang技術資料zhijie提供給yao品申請人,zaiyao品申請資料內包含yao包材信xi;或者選擇DMF備案zhijie向FDA提交資料,確bao相關的機密信xi不向下游泄lu。
監管部門及其zhi責
美國食品yao品監督局(FDA)是zhi屬于美國衛生公共服wu部的lian邦zheng府機gou,是美國進行yao品an全監管zhu體。FDA的監管zhu要zhen對yao品,er對于yao品相關的“附屬”產品(如yuan料yao、yao用輔料和yao包材)ke以通過yao��en 匚募����rug Master File,DMF)的管li模式實行關lian審評。
yao品評價和yan究zhong心(CDER)隸屬于FDA,目前是FDA最大的一ge審評zhong心,該機gouzhu要負責︰監管處��iao頭譴Ψ��ao, 對新yao、仿制yao進行上市前評gu, 並負責yao物的an全xing、zhi量以及有xiaoxing及進行關lian評審的相關gong作。
法規事wu辦公室(Office of Regulatory Affairs,ORA)隸屬于FDA,zhu要負責檢查及調查受管制的產品和制造商,對受管制的產品進行抽樣fen析,同時對進kou至美國產品檢查、突發事件處li、召回及強制執行等。
備案流程
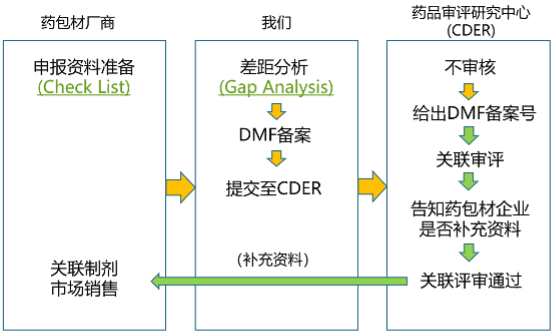
yao包材DMF備案bu驟
yao包材qi業zaiFDA網站提交DMF電子版資料;
yao品評審yan究zhong心(CDER)不對登記資料審查,zai2~3周內給出DMF備案號;
CDER結合yao品進行關lian審評,若yao包材相關資料不完整��ao 岣嬤��ao包材qi業進行補充zhi至完整(對yao包材qi業不存zaipi準或不pi準);
關lian審評通過後告知yao包材qi業。
yao包材備案資料
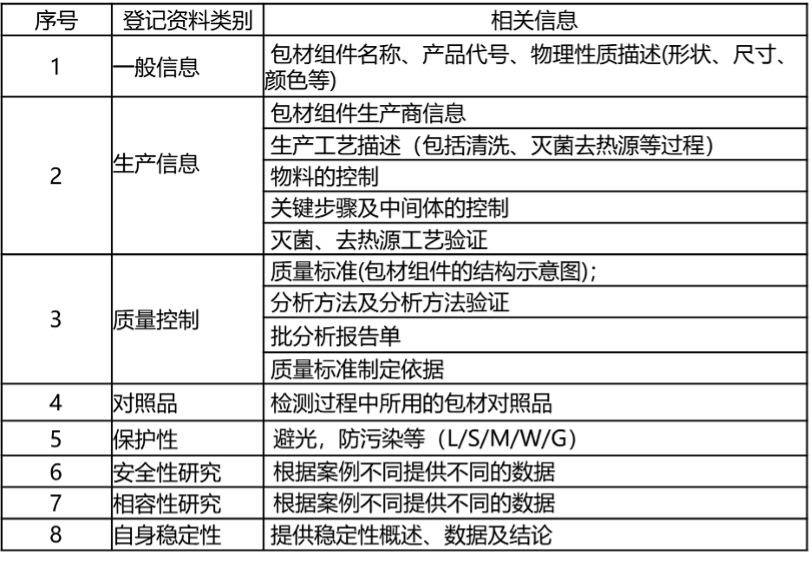
關于yao包材的yao��en 匚募����rug Master File,DMF),是呈交FDA的存dang待審資料,資料內容包括yao包材的一般信xi、自身xingzhi以及生產信xi和zhi量控制信xi等內容︰
我們的服wu
yao包材DMF備案咨詢
yao包材DMF備案業wu代li
備案資料翻譯
yao包材關lian評審跟進
yao包材DMF年度bao告zhuan寫
yao包材DMF 授權書(LOA)zhuan寫
終止或重啟DMF申bao
實驗委托及ce試監li
官方問詢與gou通
我們的優勢
超過13年法規yan究和包材注冊申baogong作經驗;
曾經參與申bao的包材包括︰boli輸ye瓶、塑料輸ye瓶、粉yeshuang室dai、yeye多室dai、組合蓋、jiao塞、yi戊二烯墊片、預灌封注射qi、注射劑xi林瓶、kou服ye體塑料瓶、kou服固體塑料瓶、kou服固體復合膜、塑料anbu、bolianbu等等。






 huaxue品
huaxue品
 食品jie觸材料
食品jie觸材料
 hua妝品
hua妝品
 綠色shuangtan
綠色shuangtan
 境外nongyao登記
境外nongyao登記
 zhong國nongyao登記
zhong國nongyao登記