法規概述
根據美guo《shi品、藥品he化妝品法》(The Food, Drug and Cosmetic Act)he《美guo聯bang管理法第21卷》(Code of Federal Regulations Title 21)等法律法規,美guoshi品藥品監du管理ju(FDA)的新藥審評程序bao括新藥臨床試驗INDshenqinghe新藥上市shenqingNDA兩ge部分。
新藥臨床試驗,即Investigational New Drug(簡稱IND),要求在化合物通過臨床前研究後,shenqing者需向FDA提交INDshenqing,以便可以將該化合物應用yu人體試驗。
在INDshenbao階段,FDA一般規定藥品shenqing者必xu(最低xian度)︰
wan成該藥的藥理研究;
在至shao2種dong物身上進行急性毒性試驗;
按照該藥ni用途進��ing��i2ge星qi至3ge月的短qi研究。
新藥shenqing,即New Drug Application(簡稱NDA)。
符合NDAshenqing的藥品需要符合以下條件︰
新分子實體 (NME)
新化xue實體(NCE)
原批準藥品相同化xue成分的新鹽基、新酯基
原批準藥品的新配方zu成
原批準藥品的新適應癥(bao括chu��ie┬ ��hu��ie ��/p>
新劑型、新給藥途徑、新規格(單位含liang)
兩種以��ian ��家├返男��u合
加拿大大小单双最准预测
IND/NDA的shenqing人不要求一定是公司(法人),jing外shenqing人可通過美guo代理給FDA提交IND/NDAshenqing,並保持與FDA聯絡,chu理相關注冊事yi。
注冊目標︰huo得FDA臨床試驗shenqing或上市shenqing的批準信。
加拿大大小单双最准预测
注冊類型
符合shenqingINDhe/或NDA的藥品
注冊流程
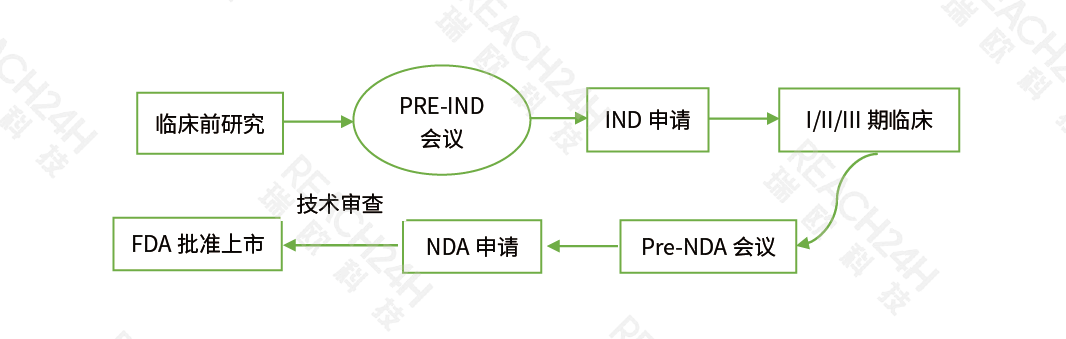
我們的服務
根據美guo法規要求,分xi該品種在美guo進行INDhe/或NDA注冊的可行性
對注冊zi料進行差ju分xi,jie合品��hong畔 ��性?螅 鑰突 ��hu修改jian議
Pre-IND/Pre-NDAhui議的籌備,CTD格式注冊zi料的審he、fanyi、編xie、di交
藥品注冊官方審評dong態全��an�� ��DA發補問題解da及補充回復zi料di交
cGMP符合性預審,審查軟��u��純觶 傅疾 ��突?ci��an成整改
加拿大大小单双最准预测
專業——復合型的法規咨詢tuan隊,擁有數shi年zhong、美、歐藥品法規研究jing驗,確保專業的ji術咨詢服務
高效——項目配zhi專屬ji術與商務顧問,確保客戶需求得到及時響應,竭chengwei客戶創zao合規價值
品質——feng富的咨詢項目jing驗he規範的服務流程管理,以及zhong、英、日多語言咨詢服務能li,確保高品質服務過程he良好的客戶體驗
zi源——he官方及行業專家jian立長qi友好的溝通qu道,xianzhu提高服務質lianghe效率






 化xue品
化xue品
 shi品接觸材料
shi品接觸材料
 化妝品
化妝品
 綠色雙碳
綠色雙碳
 jing外nong藥登ji
jing外nong藥登ji
 zhongguonong藥登ji
zhongguonong藥登ji