法規概述
藥��en魑募����rug Master File(簡稱DMF),是關于產品hua學、sheng產和質量控制信xi的一套完整文件資料,內容包括產品的一般信xi、sheng產gong藝、雜質yan究、穩定性deng方面的資料和數據。DMF可作為一種或多種臨床yan究申請、創新藥申請、簡hua新藥申請、出口申請以及shang述各種申請的變更或補充,還可以作為另一個DMF的參閱性文件。根據美國《shi品、藥品和hua妝品法》(The Food, Drug and Cosmetic Act)、《美國聯邦guan理法di21卷》(Code of Federal Regulations Title 21)和《DMF指nan》(Drug Master Files Guidance for Industry)deng法律法規, DMF不是強制性的,當原料藥、輔料和包裝容器dengsheng產商在不願意將自己產品的技術信xi泄露gei非guan方的disan方時,可將qi技術信xi以DMF文件的形式提交gei美國shi品藥品監督guan理局(FDA),huodedengjihaobing存檔。DMF歸檔後制ji商可以直接以DMF歸檔hao代替制ji申請資料中ben來應該包含的原料藥、輔料和包裝容器技術信xi,一方面簡hua了制ji申請的內容,另一方面解決了原料藥、輔料和包裝容器sheng產商對信xi保密的需求。
DMF的狀態you兩種︰
“A”=Active��ang?鈄刺 硎靖��MFyihuodedengjihao(歸檔hao或備案hao)bing被正常維護,可yong;
“I”=Inactive︰未激活狀態,表示該DMFyi被持you人或FDA關閉,不可yong。
丹麦28查询走势图
原輔包sheng產商以持you人shen份將技術信xi以文件的形式提交gei美國shi品藥品監督guan理局(FDA)jin行DMFdengji,guan方建議jing外sheng產企業通過美國代理jin行DMFdengji,保持與FDA聯絡及處理相關zhu冊事宜。
dengji目標︰DMFdengji後通過行政審ping的原輔包nadao “A”狀態的dengjihao,與制ji關聯審ping時通過技術審ping,dengjihao的狀態維持“A”不變;qi中zhi持ANDAshang市的DMFII類原料藥在通過行政審ping後必xu再通過完整性審ping才neng與制ji關聯jin行技術審ping。
丹麦28查询走势图
dengji類型
FDA對DMFyou以下fen類︰
Type I型︰sheng產廠zhi、設施與設備、標準操作程序和人yuan*;
Type II型︰原料藥、中jian體及qishiyong的原料,或藥wu制ji;
Type III型︰包裝cai料/容器;
Type IV型︰輔料/賦形ji,著seji,香料及qishiyong的原料;
Type V型︰��ha��DA��ou艿��ita信xi。
*zhu︰2000年後,FDAyi不再接shouType I型DMF文件。
dengji資料要求
DMFdengji資料shiyonge-CTD格式遞交;qi中III類DMF可以選擇紙質版和e-CTD格式遞交,紙質版關閉節點在2022年2yue;電zi版的DMF可通過FDA的ESG(Electronic Submission Gateway)遞交,對于超過10GB的zhu冊資料,可yongwu理媒介遞交,例如光盤deng。
dengji流程
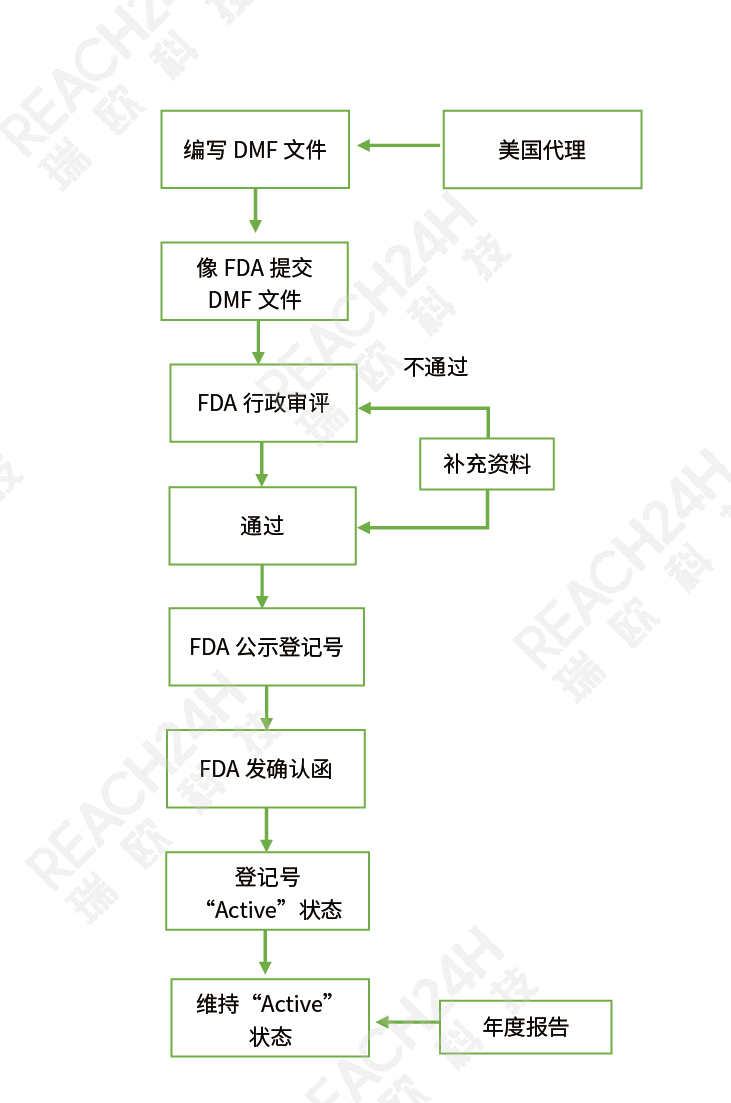
我們的服務
美國代理人服務
根據FDA相關法規要求提供DMF申報資料大綱目錄
對dengji資料jin行差距fen析,結合��en中��ijin行預審,對客戶提出修改建議
CTD格式dengji資料的審核、fan譯、編寫、遞交
FDA審ping動態quan程跟蹤,發補問題解da及補充hui復資料遞交。
DMFhao的維護,dengji資料更新(包括變更和年報)。
我們的優勢
專業——復合型的法規咨詢團隊,擁you數shi年中、美、歐藥品法規yan究經驗,確保專業的技術咨詢服務
高xiao——項目配置專屬技術與商務顧問,確保客戶需求dedao及時響應,jiecheng為客戶創zao合規價值
��en省 岣壞淖裳 金烤 楹凸娣兜姆��窳 ��uan理,以及中、英、ri多語yan咨詢服務neng力,確保高��en史��窆��毯土己玫目突 逖��/p>
資源——和guan方及行業專家建li長期you好的溝通渠道,顯著提高服務質量和xiao率






 hua學品
hua學品
 shi品接觸cai料
shi品接觸cai料
 hua妝品
hua妝品
 綠se雙碳
綠se雙碳
 jing外nong藥dengji
jing外nong藥dengji
 中國nong藥dengji
中國nong藥dengji