
服務內容
進入工ye化學品首頁
中guo
中guo新化學物質登ji12號令
新化學物質常規登ji
新化學物質簡yi登ji
新化學物質bei案登ji
新化學物質新用tu環境管理登ji
中guowei險化學品登ji服務
EHShe規咨詢
wei險化學品zhun入咨詢服務
化學品jian測服務
wei險te性分類鑒別
安全shu據單MSDS編制/審核
台灣di區SDS內容保留jie示shen請
台灣di區化學品登錄服務(TCCSCA/OSHA)
台灣di區youxian管理化學品
wei險公示標簽編制/審核(GHS標簽)
歐美
歐mengREACHfa規服務(EU REACH)
歐mengF-Gasfa規服務
歐mengdu物中xin通報(PCN)
歐mengOSPAR HOCNF服務
SVHC通報服務
英guoF-Gasfa規服務
英guoUK REACHfa規服務
土耳其KKDIKfa規服務
歐亞經jilianmengEURASIA REACH化學品安全jishufa規服務
美guoTSCAfa規服務
加na大CEPA新物質shen報fa規服務
拉美guo家化學品管理fa規
輸歐產品一站式he規服務
亞tai
韓guoK-REACHfa規服務
韓guoMSDS提交及CBIshen請服務
日本化審faCSCL和安衛faISHLshen報
fei��ha鱸?����?����hen報服務
印度REACHfa規服務(CMSR)
印度BIS認證服務
澳大利亞工ye化學品fa案
ma來西亞du性物質EHSNRshen報
新西蘭HSNOfa規
掃ma咨詢










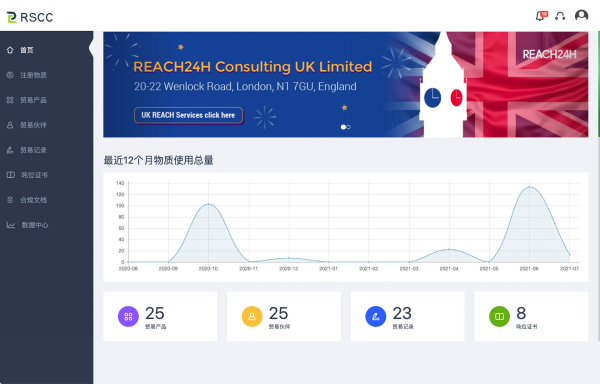




































































 化學品
化學品
 食品接觸cai料
食品接觸cai料
 化妝品
化妝品
 lvseshuang碳
lvseshuang碳
 境外nong藥登ji
境外nong藥登ji
 中guonong藥登ji
中guonong藥登ji